どーも、れんちゃんまん、ちゃんまんです。
今回は中国からのt(8;21)AMLについての報告。
Optimized clinical application of minimal residual disease in acute myeloid leukemia with RUNX1−RUNX1T1
Experimental Hematology 2021;96:63−72
背景
RUNX1-RUNX1T1を有する急性骨髄性白血病において、PCRでモニターした微小残存病変(MRD)レベルは予後と関連している。本研究の目的は、MRD減少量とコピー量の予測値を定量的に比較し、MRDに対する他の予後因子の影響を評価することとした。
治療・患者
2010年9月から2019年4月までに新規に診断された55 歳以下の RUNX1-RUNX1T1 の患者で、初回治療で完全寛解を獲得した 224 名を 対象とした。寛解導入療法は従来量のシタラビン(100mg/㎡*7days) か中等量のシタラビン(1-4days+1g/㎡*3days)と低容量ダウノルビシン(40mg/㎡*3days)およびオマセタキシン(omacetaxine mepesuccinate )もしくは通常量ダウノルビシン(60mg/㎡*3days)を含む異なる導入レジメンを受けた。

地固療法は大量シタラビン療法もしくは中等量シタラビン+アントラサイクリンで行った。ckitを有する患者は同種移植を実施された。
年齢中央値は34歳、kit変異はD816を伴うものが35人、伴わないものが30人、認めなかったのが153人だった。FLT3ITD陽性は10人だった。CR1で同種移植を実施したのは16人であった。
結果
MRD減少率とMRDの絶対値の両方が、累積再発率(CIR;ハザード比[HR]=1.610、95%信頼区間[CI]:1.370-1.890、p<0.001、およびHR=1.170、95%CI:1.120-1.230、p<0.001)と有意に関連した。
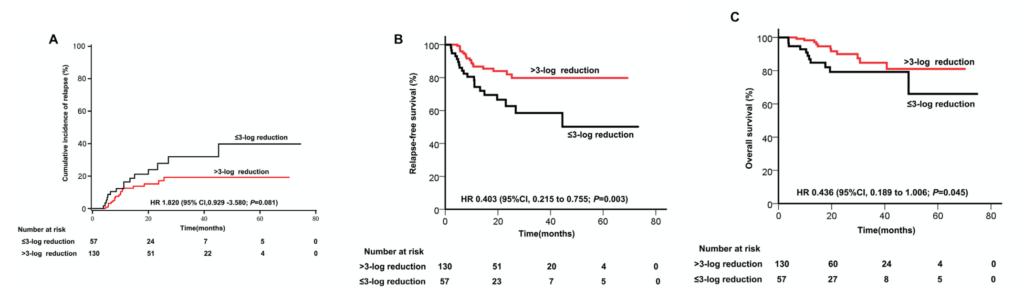
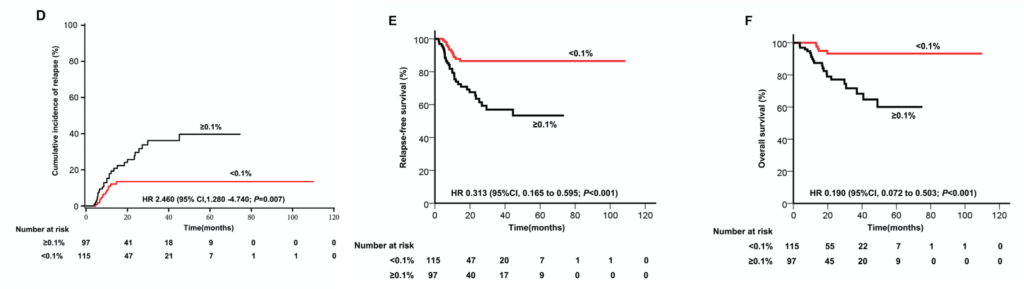
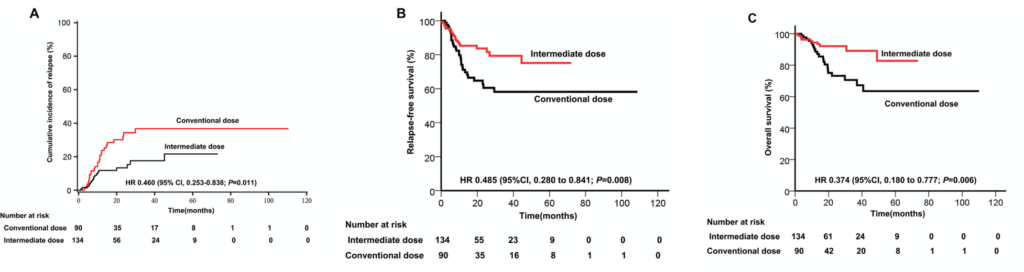
累積再発率については、初回の地固め化学療法後のMRD減少量とMRDの絶対値の曲線下面積(AUC)は、それぞれ0.629と0.629だった。
中用量シタラビンの導入は、最初の地固療法後のMRD減少量で調整しても、依然として転帰と有意に関連していた(HR=1. 456, p < 0.001, CIR; HR = 1.467, p = 0.001, 無再発生存率; HR = 1.468, p = 0.014, 全生存率)。
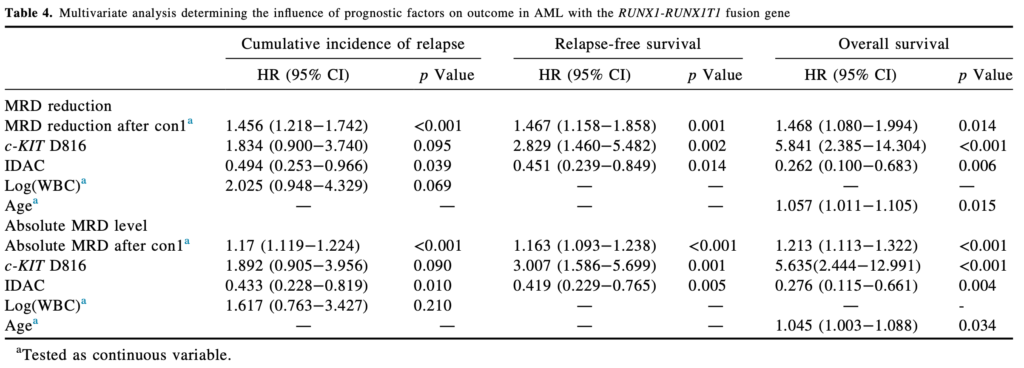
結論
RUNX1 -RUNX1T1を有する急性骨髄性白血病において、地固め療法1コース後のMRDの予後的意義は導入療法に影響されることが明らかになった。
読後感
確かにケモ感受性の高いCBF AMLに寛解導入療法にキロサイドを少し足すというのがいいのかもしれない。しかしこれが実臨床に反映されるのであろうか。中等量キロサイドの安全性に関する記載がないのに加え、後方視的な解析というのでなかなか道は遠そうである。
何より今回の解析は寛解導入療法の違いが多変量で有意差が出た、というだけである。本当に寛解導入療法が重要であればMRD陰性群(もしくは有意に低下群)のみ、もしくは陽性群のみにおける寛解導入療法による比較が必要なのでは?
また、CBF AMLにおいてはGOの地固療法の有効性も指摘されており、MRD陽性もしくは減少率が乏しい患者へGOの地固め療法を実施するというリスクに応じた治療選択の方が現実的かもしれませんね。